سلامت
2 دقیقه پیش | نشانه ها و عوارض کمبود ویتامینها در بدنویتامینها نقش مهمی را در بدن انسان ایفا میکنند. بهنحویکه کمبود ویتامین (حتی یکی از آنها) میتواند برای هر فردی مشکلات اساسی را به وجود آورد. گجت نیوز - معین ... |
2 دقیقه پیش | چرا پشه ها بعضی ها را بیشتر نیش میزنند؟فصل گرما و گزیده شدن توسط پشه ها فرا رسیده، دوست دارید بدانید پشه ها بیشتر چه کسانی را دوست دارند؟ بیشتر کجاها می پلکند؟ و از چه مواد دفع کننده ای نفرت دارند؟ وب سایت ... |
بیماری فروید
در چند دهه اخیر، میانگین سن بیماران سرطان دهان 60 سال بود ولی امروزه این میانگین سنی پایین آمده و شاهد ابتلای جوانان به توده هایی در حفره دهان هستیم.
مجله سلامت - پرنیان پناهی: در چند دهه اخیر، میانگین سن بیماران سرطان دهان 60 سال بود ولی امروزه این میانگین سنی پایین آمده و شاهد ابتلای جوانان به توده هایی در حفره دهان هستیم. در «دهان و دندان» این هفته درباره توده های بدخیم دهانی با دکتر محسن نراقی، فلوشیپ فوق تخصصی راینولوژی و دانشیار دانشگاه علوم پزشکی تهران گفتگو کرده ایم.
چرا توده های دهانی دیر تشخیص داده می شوند؟
- علت اینکه ضایعات بدخیم دهانی با تاخیر تشخیص داده می شوند، شیوع زیاد ضایعات خوش خیم دهانی مانند زخم های آفتی و ... است که برای بیمار شبهه ایجاد می کند که این ضایعه هم مانند ضایعات قبلی خود به خود برطرف خواهد شد در حالی که ضایعات بدخیم برطرف نمی شوند مگر با درمان جراحی؛ بنابراین ضایعاتی دهانی که بیش از 15-10 روز در دهان باقی بمانند، حتما به بررسی نیاز دارند.
سرطان های حفره دهانی بیشتر از چه نوعی هستند؟
- شایع ترین نوع تومورها، سلول های سنگفرشی حفره دهانی را درگیر می کند ولی ابتلا به این نوع سرطان ها معمولا اتفاقی نیست و در افرادی اتفاق می افتد که عامل خطر را داشته باشند.
چه عوامل خطری؟
- مهمترین عامل مرتبط با سرطان حفره دهانی مصرف سیگار و الکل است. البته الکل تقویت کننده اثر سرطانزایی سیگار است؛ یعنی احتمال ابتلای مرد یا زنی که سیگار می کشد به ترتیب 2 برابر و 3 برابر بالا می رود.
این خطر با تعداد سیگار در روز و سال های استعمال آن ارتباط مستقیم دارد. الکل نیز به تنهایی احتمال ابتلا به این سرطان را 2 تا 3 برابر می کند اما در کسانی که هم سیگار می کشند و هم الکل مصرف می کنند، این احتمال به 35 برابر افزایش می یابد. بعضی از سیگاری ها هم عادت دارند سیگا ررا به طور معکوس در دهان قرار دهند که عمل بسیار خطرناکی است. چنین افرادی 47 برابر غیرسیگاری ها در معرض خطر سرطان کام سخت قرار دارند و ویروسی نیز به نام پاپیلومای انسانی که ارتباط نزدیکی با سرطان دهانه رحم دارد در سرطان های سلول های سنگفرشی سر و گردن نقش دارد.
تماس با اشعه فرابنفش خورشیدنیز در ایجاد سرطان لب نقش دارد؛ به خصوص در کسانی که لب پایین شان بیش از حد به جلو متمایل شده و حاشیه لب پایین در معرض نور خورشید قرار گرفته است. افرادی که پیپ می کشند و لب با مواد شیمیایی و سمی در تماس است هم در معرض ابتلا به سرطان لب هستند.
آیا ضایعات سرطانی از ابتدا ماهیت سرطانی دارند یا بعد به سرطان تبدیل می شوند؟
- بعضی از ضایعات سرطان نیستند ولی به ضایعات پیش بدخیم حفره دهانی معروف اند و لکوپلاتی نام دارند. نمای مخاطی سفید ضایعه سفید است و از بافت زیرین جدا نمی شود. خطر پیشرفت به سمت بدخیم در این ضایعات 7 برابر است.
آیا ضایعات بدخیم همیشه بی علامت هستند؟
- هر چه بیماری بیشتر پیشروی کند، علامت های آن هم متنوع تر می شود. سفتی هنگام باز کردن دهان، دردهای دهانی - دندانی، بوی بد دهان، تغییر تناسب دندان های مصنوعی قبلی، اختلال در بلع، اختلال در تکلم و بی حسی در صورت و کاهش وزن و خونریزی از علائم تومورهای دهانی است.
چگونه می توان تشخیص داد تومور سرطانی است؟
- بعد از معاینه و گرفتن شرح حال کامل از بیمار، پرسیدن بیماری های قبلی، استعمال دخانیات و مصرف الکل، به نمونه برداری از حاشیه تومور نیاز است. با عکسبرداری وسعت بیماری و گسترش تومور به لنف ها ارزیابی می شود.
درمان جراحی است؟
- بله، درمان جراحی است و جراحی اش هم 3 نوع است که جراح براساس نوع تومور و منطقه درگیر و عمق آن تصمیم می گیرد که چگونه تومور را خارج کند. بعضی از بیماران به دلیل گسترش تومور به اطراف به پرتودرمانی هم نیاز دارند.
آیا بعد از درمان کامل احتمال عود بیماری وجود دارد؟
- در بیمارانی که علت تومورشان، کشیدن سیگار تشخیص داده شود، احتمال مجدد پیداش تومور بعدی وجود دارد. از هر 7 بیمار مبتلا به بدخیمی اولیه، در سر و گردن یک نفر به تومور اولیه بعدی مبتلا می شود. بیشتر عودها طی 2 سال اول ظاهر می شوند. محل بدخیمی بعدی در بیمارانی که به سرطان حفره دهان مبتلا هستند، مری در ناحیه گردن است. به همین دلیل چنین بیمارانی به محض اشکال در بلع نیاز است ارزیابی تشخیصی شوند.
فروید، سیگار برگ و سرطان دهان
زیگموند فروید، عصب شناس سرشناس اتریشی که پدر علم روانکاوی شناخته می شود، در فوریه 1923 به دلیل افراط در کشیدن سیگار برگ، دچار سرطان دهان شد. او ابتدا این مسئله را به صورت راز نگه داشت اما بالاخره موضوع را با یکی از دوستانش که جراح بود، در میان گذاشت.
دکتر به او گفت که توده باید برداشته شود. فروید با یک متخصص پوست که از دوستانش بود نیز مشورت کرد و از زبان او شنید که حتما باید سیگارش را ترک کند اما او نیز درباره جدی بودن سرطانش چیزی نگفت.
فروید بعد از مدتی به دیدن پزشکی رفت که سرطان او را تهاجمی تشخیص داده بود و از زبان او نیز شنید که برای جلوگیری از رشد سرطانش باید سیگار را ترک کند. بالاخره توسط یک متخصص گوش، حلق و بینی که فروید صلاحیت فردی، اجتماعی نه پزشکی او را زیر سوال برده بود، تحت درمان قرار گرفت.
او قبل و بعد از عمل دچار خونریزی شد و به سختی از مرگ جان سالم به در برد. پس از عمل هم به صورت مرتب توسط جراح اولش ویزیت شد. در اثنای همین ویزیت ها متوجه شد که عمل های بعدی نیز باید انجام بگیرد اما جراحش از گفتن این حقیقت به فروید خودداری می کرد چرا که فکر می کرد اگر او متوجه مسئله شود، ممکن است دست به خودکشی بزند.
بالاخره اواسط سپتامبر 1939 سرطان سقف دهان فروید باعث درد شدیدی شد و پزشکان به او اعلام کردند که توده اش قابل جراحی نیست. آخرین کتابی که او خواند، چرم ساغری بالزاک بود که باعث شد مدتی از ادامه درمان سر باز بزند اما بالاخره مدتی بعد نزد پزشکش رفت و به او گفت: «قرارمان را که فراموش نکرده ای؟ من به آخر خط رسیده ام یا نه؟ قرار بود با من صادق باشی و تنهایم نگذاری.»
دوستش به او اطمینان داد که قرارشان یادش نرفته و فروید به درمان ادامه داد... پس از کش و قوس هایی بالاخره فروید در 23 سپتامبر 1939 از دنیا رفت.
آنچه درباره سرطان فروید جالب توجه است، توجه به این نکته است که از زمان تشخیص بیماری اش در فوریه 1923 تا زمان مرگش در 23 سپتامبر 1939 او به مدت 16 سال با سرطانش جنگید و توانست بیماری اش را مدیریت کند.
ویدیو مرتبط :
ساختار شخصیت از نظر فروید
خواندن این مطلب را به شما پیشنهاد میکنیم :
تالاسمی یک بیماری ارثی-ژنتیکی

تالاسمی نوعی کم خونی ارثی و ژنتیکی است که به علت اشکال در ساخت زنجیرههای پروتئینی هموگلوبین بوجود میآید.هموگلوبین مولکول اصلی داخل گویچههای قرمز است که از هم و زنجیرههای پروتئنی یا گلوبین تشکیل شده است. در هر زنجیره گلوبین یک مولکول هم وجود دارد که اکسیژن را توسط آهن خود حمل میکند. پس تولید هموگلوبین نیاز به تامین آهن و ساخت هموگلوبین دارد بر اساس نوع زنجیره پروتئینی چند نوع هموگلوبین وجود دارد:
هموگلوبین A: هموگلوبین طبیعی در بالغین عمدتا همولگوبین A میباشد که تقریبا حدود 98% از هموگلوبین جریان خون را تشکیل میدهد و از زنجیره 4 تایی حاوی دو زنجیره آلفا و دو زنجیره بتا ساخته میشود. (α2β2)
HGbA2: هموگلوبین A2 از 2 زنجیره آلفا و 2زنجیره بتا تشکیل میشود.(α2δ2) که بطور طبیعی 2-1% هموگلوبین در بالغین را تشکیل میدهد.
HGbF: هموگلوبین F که هموگلوبین اصلی دوران جنینی است و کمتر از 1% هموگلوبین در بالغین را نیز شامل میشود،از زنجیره 4 تایی 2 تا آلفا و 2 تا گاما (α2δ2) تشکیل گردیده است و هموگلوبین های C , H و ... که در بعضی بیماریها بوجود میآید.
برای ساخت زنجیره بتا هر فرد از هر والد خود (پدر و مادر) یک ژن سازنده این زنجیره را دریافت میکند و برای زنجیرههای δ,α از هر والد 2 ژن دریافت میکند. و بر اساس جهش یا حذف هر کدام از این ژنها ساخت و زنجیره مربوطه مختل شده و انواع بیماری تالاسمی را خواهیم داشت.
هموگلوبین نه تنها برای حمل و تحویل طبیعی اکسیژن لازم است، بلکه در شکل و اندازه و بدشکلی گلبول قرمز دخالت دارد. مقدار کل هموگلوبین خون بطور طبیعی در خانمها 2±12 و در آقایان 2±14 گرم در دسیلیتر میباشد.
انواع تالاسمی
تالاسمی به دو نوع آلفا تالاسمی و بتا تالاسمی است که خود بتا تالاسمی هم شامل تالاسمی ماژور (تالاسمی شدید) و تالاسمی مینور یا تالاسمی خفیف میباشد. افراد مبتلا به تالاسمی مینور در واقع کم خونی مشکلسازی ندارندریا، ولی اگر دو فرد تالاسمی مینور با هم ازدواج کنند به احتمال 25% فرزندنشان دچار تالاسمی شدید ماژور خواهد بود و 25% فرزندشان سالم و 50% تالاسمی مینور خواهند داشت.
تالاسمی ماژور
تالاسمی ماژور یا آنمی کولی به علت حذف یا جهش در هر دو ژن سازنده زنجیره بتا ایجاد میشود و به این ترتیب یا هیچ زنجیره بتایی ساخته نمیشود و یا به مقدار کمی ساخته میشود. در نتیجه بدن کمبود این زنجیرهها را با ساخت زنجیرههای آلفا جبران میکند که این زنجیرههای آلفای اضافی برای گلبولهای قرمز سمی هستند و با رسوب بر روی سلولهای گلبول قرمز باعث میشوند که گلبولهای قرمز در مغز استخوان و در داخل خون تخریب شده و زنجیرههای آلفا در مغز استخوان رسوب میکنند. از طرفی به علت خونسازی غیر موثر ، مراکز خونساز خارج مغز استخوان ، ار جمله کبد و طحال شروع به خونسازی میکنند و بزرگ میشوند.
بیماری معمولا بصورت کم خونی شدید در 6 ماهه اول زندگی کودک تظاهر میکند و درصورت عدم شروع تزریق خون ، بافت مغز استخوان و مکانهای خونساز خارج مغز استخوان فعال و بزرگ شده و باعث بزرگی مغز استخوانها بخصوص استخوانهای پهن (صورت و جمجمه) و بزرگی کبد و طحال میشوند.

علایم بیماری
کم خونی شدید طوریکه برای بقاء بیمار تزریق مکرر خون لازم است.
افزایش حجم شدید مغز استخ
وان بخصوص در استخوانهای صورت و جمجمه ، چهره خاص افراد تالاسمی را ایجاد میکند (چهره موش خرمایی).
اختلال رشد دربچههای بزرگتر
رنگ پریدگی ، زردی و گاهی پوست ممکن است به دلیل رنگ پریدگی و یرقان و رسوب ملانین به رنگ مس در آید.
بزرگی کبد و طحال ، در سنین بالاتر گاهی طحال به حدی بزرگ میشود که باعث تخریب بیشتر گلبولهای قرمز میشود.
علایم ناشی از رسوب آهن در بافتهای مختلف از جمله پانکراس و قلب و غدد جنسی و ایجاد دیابت و نارسایی قلبی و تاخیر در بلوغ.
استخوانها نازک شده و مستعد شکستگی میشوند.
تشخیص
در آزمایش خون تالاسمی ماژور گلبولهای قرمز خون کوچک و کم رنگ خواهد بود (کم خونی هیپوکروم میکروسیتر). افت شدید هموگلوبین به مقادیر کمتر از 5 گرم در دسی لیتر وجود دارد. بیلی روبین سرم به علت تخریب سلولها افزایش مییابد و سایر آزمایشات که لزومی برای گفتن همه آنها نیست. تشخیص قطعی با الکتروفورز هموگلوبین انجام میشود که در تالاسمی ماژور هموگلوبین A طبیعی ساخته نمیشود و 98% هموگلوبینها را هموگلوبین F تشکیل میدهد و هموگلوبین A2 نیز تا 5% افزایش پیدا میکند.
عوارض
از عوارض تالاسمی یک سری از عوارض از جمله اختلال رشد و تغییر قیافه بیمار و بزرگی کبد و طحال که به علت خود بیماری است و یکسری عوارض دیگر ناشی از درمان تالاسمی است. اصلیترین این عارضه هموسیدوز یا هموکروماتوز است.
هموسیدروز به رسوب آهن در بافتها گفته میشود که نتیجه غیر قابل اجتناب تزریق طولانی مدت خون است. در هم نیم لیتر خونی که به بیمار تزریق میشود، حدود 200mg آهن به بافتها منتقل میکند که این مقدار آهن نمیتواند از بدن دفع شود و در بافتها رسوب میکند و باعث نارسایی در بافتها میگردد. بخصوص رسوب آهن در قلب و پانکراس و غدد ، مشکل اصلی این بیماران خواهد بود که باعث نارسایی پانکراس و دیابت ، نارسایی قلبی و نارسایی غدد جنسی و تیروئید و ... میشود.
درمان
تالاسمی شدید و درمان نشده همیشه باعث مرگ در دوران کودکی میگردد. در صورت تزریق مکرر خون و حفظ سطح مناسبی از خون میتوان طول عمر ا افزایش داد و تا حد زیادی مانع از تغییرات استخوانی و اختلال رشد گردید. پس درمان تالاسمی عبارتند از:
تزریق دراز مدت خون: هدف از تزریق خون مکرر برای بیمار حفظ هموگلوبین بیمار در سطح بالای 10 است.
دفروکسامین: مشکل اصلی بیماران تالاسمی بعد از سالها ، هموسیدروز و اضافه بار آهن است، که میتوان آن را به کمک تزریق مرتب دفروکسامین به صورت زیر جلدی یا وریدی تخفیف داد. این دارو با آهن ترکیب شده و از ادرار دفع میشود. البته مقدار زیاد این دارو ممکن است باعث واکنش پوستی در محل تزریق و یا عوارض عصبی به ویژه در دستگاه بینایی و شنوایی شود. بنابراین این دارو به تنهایی برای پیشگیری دراز مدت از مسمومیت با آهن کافی نیست.
برداشتن طحال: اگر بزرگی طحال ، نیاز به تزریق خون را بیشتر کند طحال برداشته میشود تا نیاز به خون کاهش یابد.
پیوند مغز استخوان: درمان قطعی بیماری با پیوند مغز استخوان است. البته این عمل با مرگ ومیر بالایی همراه است. و در برخی بیماران نیز سلولهای تالاسمی مجددا رشد میکنند.
روند بیماری
امروزه با توجه به درمانهای موجود بیماران تا 30 سالگی هم زنده میمانند. و اینها بچههایی با رشد ناقص هستند و شایعترین علت مرگ آنها نارسایی قلبی به علت هموسیدروز و همچنین به علت تزریق خون و افزایش بار قلب میباشد.
تالاسمی مینور
تالاسمی مینور معمولا بدون علامت بوده و علایم بالینی واضح ندارند و بطور عمده در تستهای چکاپ به صورت اتفاقی تشخیص داده میشوند. این افراد کم خونی مختصر (هموگلوبین بیش از 10) با سلولهای گلبول قرمز کوچک و کم رنگ (هیپوکروم میکروسیتر) دارند که معمولا مشکلساز نمیباشد.
تالاسمی مینور در نتیجه اختلال یکی از دو ژن سازنده زنجیره گلوبین بتا به وجود میآید که این ژن ناقص یا از پدر و یا از مادر به فرد به ارث رسیده است، در نتیجه کاهش یا فقدان ساخت زنجیره بتا از یک ژن اتفاق میافتد و به دنبال آن هموگلوبین A2 تا حدود %8-4 افزایش مییابد و گاهی افزایش هموگلوبین F در حدود %1-5 دیده میشود.
تنها نکتهای که در تالاسمی خفیف یا مینور جالب توجه است، این است که این افراد موقع ازدواج نباید با یک فرد شبیه خود (تالاسمی مینور) ازدواج کنند.
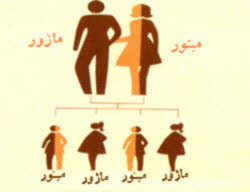
آلفا تالاسمی
علت آلفا تالاسمی حذف یک یا چند ژن از 4 ژن سازنده زنجیره آلفاست، هر چه تعداد ژنهای حذف شده بیشتر باشد بیماری شدیدتر میشود و براساس تعداد ژنهای حذف شده به 4 گروه تقسیم میشوند.
هیدروپس فتالیس: که حذف هر 4 ژن آلفا را دارند و هموگلوبین ساخته شده فقط از زنجیرههای گاما تشکیل شده است که هموگلوبین بارتز گفته میشود و وخیمترین نوع آلفا تالاسمی است و با حیات خارج رحمی منافات دارد و جنین هنگام تولد مرده است و یا مدت کوتاهی پس از تولد میمیرد. این جنینها دچار ادم شدید هستند.
بیماری هموگلوبین H: که در اثر حذف 3 ژن آلفا گلوبین بوجود میآید. بیماران دچار کم خونی هیپوکروم میکروسیتیک بوده و بزرگی طحال در آنها دیده میشود. در بعضی مواقع ممکن است نیاز به تزریق خون داشته باشند و در صورت کم خونی شدید و نیاز به انتقال خون باید طحال برداشته شود.
صفت آلفا تالاسمی 1: که 2 ژن آلفا حذف شده و از هر لحاظ شبیه بتا تالاسمی مینور است.
صفت آلفا تالاسمی 2: که فقط یک ژن از 4 ژن حذف شده و یک حالت ناقل ژن ، خاموش و بدون علامت است.
 انتخاب جراح بینی - بهترین جراح بینی
انتخاب جراح بینی - بهترین جراح بینی  عکس: استهلال ماه مبارک رمضان
عکس: استهلال ماه مبارک رمضان  عکس: ارزش تیم های حاضر در یورو 2016
عکس: ارزش تیم های حاضر در یورو 2016 