کودکان
2 دقیقه پیش | با بطری نوشابه برای پسر کوچولو هواپیما بسازیدبه جای خریدن اسباب بازی های گران قیمت ، می توانید با استفاده از ابزاری که در خانه در اختیار دارید اسباب بازی هایی با کمک فرزندان خود بسازید که هم در هزینه ها صرفه جویی می ... |
2 دقیقه پیش | از رایحه درمانی نوزادان بیشتر بدانیدآیا شما می خواهید برای مراقبت از نوزاد خود، یک رویکرد جامع تری را انتخاب کنید؟ آیا شما به عنوان یک پدر و مادر به دنبال درمان های طبیعی برای بچه های کوچک خود هستید؟ آیا می ... |
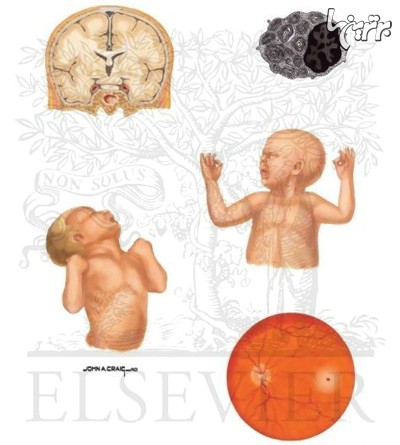
بیماری تای-ساکس چیست؟
وقتی پروتئین های چرب در مغز انباشته می شوند، به بینایی، شنوایی و رشد حرکتی و ذهنی کودک آسیب می زنند.
صبح بخیر: بینایی، شنوایی و کارکردهای حیاتی دیگر در کودکان سالم بطور طبیعی به کمک آنزیم هایی رشد می کند که پروتئین های چرب و مواد نامطلوب را از بین می برند تا در رشد تداخلی صورت نگیرد.
در کودکانی که به بیماری تای-ساکس (Tay-Sachs disease) مبتلا هستند، یکی از مهمترین آنزیم ها به نام هگزوز آمینیداز آ یا هگز آ (Hexosaminidase A) وجود ندارد. بنابراین وقتی پروتئین های چرب در مغز انباشته می شوند، به بینایی، شنوایی و رشد حرکتی و ذهنی کودک آسیب می زنند.
فقط از طریق ارث بردن است که کودک به این بیماری مبتلا می شود. البته این بیماری ارثی در میان گروه های قومی و نژادی خاصی مانند یهودیان اشکنازی، نسبتاً شایع است. بیماری تای-ساکس را می توان قبل از تولد نوزاد شناسایی کرد و زوج هایی که ریسک داشتن ژن این بیماری را دارند، باید آزمایش خون بدهند تا متوجه شوند که آیا فرزند آنها این بیماری را خواهد داشت یا خیر.
ریسک ابتلا به بیماری تای-ساکس برای کدام افراد بیشتر است؟
هر ساله حدود 16 مورد بیمار تای-ساکس در ایالات متحده شناسایی می شود. با آنکه یهودیان اشکنازی (یهودیان اروپای مرکزی و شرقی) ریسک بالاتری در ابتلا به تای-ساکس دارند، ولی این بیماری در میان جمعیت های غیریهودی مانند مردم فرانسوی-کانادایی تبار نیز شایع است.
بعضی از مردم نیز از طریق جهش ژنتیکی این بیماری را دارند. در میان یهودیان اشکنازی، یک نفر از هر 27 نفر ناقل این بیماری است، ولی در کل جمعیت دنیا، 1 نفر از هر 250 نفر به آن مبتلاست.
کودک زمانی به این بیماری مبتلا می شود که هر دوی والدین او ناقل تای-ساکس باشند. وقتی دو فرد ناقل بچه دار می شوند، احتمالات بدین قرار می شود:
• 50 درصد احتمال دارد که فرزندشان ناقل باشد، ولی این بیماری را نداشته باشد؛
• 25 درصد احتمال دارد که فرزندشان ناقل نباشد و بیماری را نداشته باشد؛
• 25 درصد احتمال دارد که فرزندشان این بیماری را داشته باشد.
نحوه نظارت بر بیماری
زوج هایی که می خواهند بچه دار شوند – یا زوجی که در انتظار فرزندی هستند – می توانند با یک آزمایش خون ساده، از داشتن یا نداشتن ژن تای-ساکس مطمئن شوند. اگر هر دوی والدین ژن تای-ساکس را داشته باشند، متخصص زنان و زایمان زوج را به مشاور ژنتیک معرفی می کند.
تشخیص قبل از زایمان
مادران باردار می توانند آزمایش بدهند تا مشخص شود که جنین آنها کمبود آنزیم هگز آ دارد یا خیر. اگر در آزمایش ها مشخص شود که جنین هگز آ ندارد، او به بیماری تای-ساکس مبتلا می شود. ولی اگر در آزمایش ها آنزیم هگز آ کشف شد، نوزاد این بیماری را نخواهد داشت.
بین هفته های دهم تا دوازدهم بارداری، مادر باردار می تواند آزمایش نمونه برداری CVS بدهد که در این آزمایش با یک سرنگ یا لوله کوچک، نمونه کوچکی از جفت گرفته می شود.
بین هفته های پانزدهم تا هجدهم بارداری، مادر می تواند آزمایش آمنیوسنتز بدهد تا از وجود یا عدم وجود ژن تای-ساکس مطمئن شود. در این آزمایش، سرنگی به شکم مادر زده می شود و نمونه ای از مایع آمنیوتیک که جنین در آن قرار دارد، گرفته می شود.
نشانه ها و علائم
وجود بیماری تای-ساکس در کودکان معمولاً از روی مشکلات بینایی، شنوایی و حرکتی تشخیص داده می شود. پزشک می تواند با معاینه فیزیکی و آزمایش خون نیز این بیماری را تشخیص دهد.
کودکی که با بیماری تای-ساکس متولد می شود معمولاً در ماه های سوم تا ششم زندگی رشد نرمالی دارد. در ماه ها – یا حتی سال های بعدی – زندگی کودک به تدریج بینایی، شنوایی و قوه حرکتی خود را از دست می دهد. نقطه قرمزی پشت چشمان کودک رشد می کند و دیگر نمی تواند لبخند بزند، بخزد، برگردد و اشیا را بردارد. در دو سالگی، کودک تشنج می کند و کاملاً فلج می شود. مرگ معمولاً در سن 5 سالگی رخ می دهد.
در انواع نادری از این بیماری، ممکن است کودک آنزیم هگز آ را داشته باشد، ولی آنقدر کافی نباشد که از مشکلات رشدی جلوگیری کند. در یکی از انواع این بیماری که Juvenile Hex A Deficiency نام دارد، این مشکلات تا سن 2 تا 5 سالگی ظاهر نمی شوند. این بیماری کندتر خودش را نشان می دهد، ولی مرگ زمانی که کودک به 15 سالگی می رسد رخ می دهد.
در نوع دیگری از این بیماری که خفیف تر از تای-ساکس است، عضلات ضعیف می شوند و تکلم کودک جویده جویده می شود، ولی بینایی، شنوایی و توانایی های ذهنی کودک مشکلی ندارند.
کمک به کودک مبتلا به تای-ساکس
هیچ درمانی برای هیچ یک از انواع بیماری تای-ساکس وجود ندارد. ولی پزشکان می توانند با تجویز داروهایی برای تسکین درد، مهار تشنج ها و انقباض عضلات، به کودک مبتلا کمک کنند.
پژوهشگران در حال مطالعه و تحقیق در مورد روش هایی برای بهبود درمان این بیماری هستند. اگر فرزند شما بیماری تای-ساکس دارد یا اینکه هم شما و هم همسرتان ناقل ژن این بیماری هستید، باید نزد مشاور ژنتیک بروید.
ویدیو مرتبط :
موی تای-وای کرو-رقص موی تای-تای بوکس-پاهویوت-تای فایتر-مبارز
خواندن این مطلب را به شما پیشنهاد میکنیم :
تالاسمی یک بیماری ارثی-ژنتیکی

تالاسمی نوعی کم خونی ارثی و ژنتیکی است که به علت اشکال در ساخت زنجیرههای پروتئینی هموگلوبین بوجود میآید.هموگلوبین مولکول اصلی داخل گویچههای قرمز است که از هم و زنجیرههای پروتئنی یا گلوبین تشکیل شده است. در هر زنجیره گلوبین یک مولکول هم وجود دارد که اکسیژن را توسط آهن خود حمل میکند. پس تولید هموگلوبین نیاز به تامین آهن و ساخت هموگلوبین دارد بر اساس نوع زنجیره پروتئینی چند نوع هموگلوبین وجود دارد:
هموگلوبین A: هموگلوبین طبیعی در بالغین عمدتا همولگوبین A میباشد که تقریبا حدود 98% از هموگلوبین جریان خون را تشکیل میدهد و از زنجیره 4 تایی حاوی دو زنجیره آلفا و دو زنجیره بتا ساخته میشود. (α2β2)
HGbA2: هموگلوبین A2 از 2 زنجیره آلفا و 2زنجیره بتا تشکیل میشود.(α2δ2) که بطور طبیعی 2-1% هموگلوبین در بالغین را تشکیل میدهد.
HGbF: هموگلوبین F که هموگلوبین اصلی دوران جنینی است و کمتر از 1% هموگلوبین در بالغین را نیز شامل میشود،از زنجیره 4 تایی 2 تا آلفا و 2 تا گاما (α2δ2) تشکیل گردیده است و هموگلوبین های C , H و ... که در بعضی بیماریها بوجود میآید.
برای ساخت زنجیره بتا هر فرد از هر والد خود (پدر و مادر) یک ژن سازنده این زنجیره را دریافت میکند و برای زنجیرههای δ,α از هر والد 2 ژن دریافت میکند. و بر اساس جهش یا حذف هر کدام از این ژنها ساخت و زنجیره مربوطه مختل شده و انواع بیماری تالاسمی را خواهیم داشت.
هموگلوبین نه تنها برای حمل و تحویل طبیعی اکسیژن لازم است، بلکه در شکل و اندازه و بدشکلی گلبول قرمز دخالت دارد. مقدار کل هموگلوبین خون بطور طبیعی در خانمها 2±12 و در آقایان 2±14 گرم در دسیلیتر میباشد.
انواع تالاسمی
تالاسمی به دو نوع آلفا تالاسمی و بتا تالاسمی است که خود بتا تالاسمی هم شامل تالاسمی ماژور (تالاسمی شدید) و تالاسمی مینور یا تالاسمی خفیف میباشد. افراد مبتلا به تالاسمی مینور در واقع کم خونی مشکلسازی ندارندریا، ولی اگر دو فرد تالاسمی مینور با هم ازدواج کنند به احتمال 25% فرزندنشان دچار تالاسمی شدید ماژور خواهد بود و 25% فرزندشان سالم و 50% تالاسمی مینور خواهند داشت.
تالاسمی ماژور
تالاسمی ماژور یا آنمی کولی به علت حذف یا جهش در هر دو ژن سازنده زنجیره بتا ایجاد میشود و به این ترتیب یا هیچ زنجیره بتایی ساخته نمیشود و یا به مقدار کمی ساخته میشود. در نتیجه بدن کمبود این زنجیرهها را با ساخت زنجیرههای آلفا جبران میکند که این زنجیرههای آلفای اضافی برای گلبولهای قرمز سمی هستند و با رسوب بر روی سلولهای گلبول قرمز باعث میشوند که گلبولهای قرمز در مغز استخوان و در داخل خون تخریب شده و زنجیرههای آلفا در مغز استخوان رسوب میکنند. از طرفی به علت خونسازی غیر موثر ، مراکز خونساز خارج مغز استخوان ، ار جمله کبد و طحال شروع به خونسازی میکنند و بزرگ میشوند.
بیماری معمولا بصورت کم خونی شدید در 6 ماهه اول زندگی کودک تظاهر میکند و درصورت عدم شروع تزریق خون ، بافت مغز استخوان و مکانهای خونساز خارج مغز استخوان فعال و بزرگ شده و باعث بزرگی مغز استخوانها بخصوص استخوانهای پهن (صورت و جمجمه) و بزرگی کبد و طحال میشوند.

علایم بیماری
کم خونی شدید طوریکه برای بقاء بیمار تزریق مکرر خون لازم است.
افزایش حجم شدید مغز استخ
وان بخصوص در استخوانهای صورت و جمجمه ، چهره خاص افراد تالاسمی را ایجاد میکند (چهره موش خرمایی).
اختلال رشد دربچههای بزرگتر
رنگ پریدگی ، زردی و گاهی پوست ممکن است به دلیل رنگ پریدگی و یرقان و رسوب ملانین به رنگ مس در آید.
بزرگی کبد و طحال ، در سنین بالاتر گاهی طحال به حدی بزرگ میشود که باعث تخریب بیشتر گلبولهای قرمز میشود.
علایم ناشی از رسوب آهن در بافتهای مختلف از جمله پانکراس و قلب و غدد جنسی و ایجاد دیابت و نارسایی قلبی و تاخیر در بلوغ.
استخوانها نازک شده و مستعد شکستگی میشوند.
تشخیص
در آزمایش خون تالاسمی ماژور گلبولهای قرمز خون کوچک و کم رنگ خواهد بود (کم خونی هیپوکروم میکروسیتر). افت شدید هموگلوبین به مقادیر کمتر از 5 گرم در دسی لیتر وجود دارد. بیلی روبین سرم به علت تخریب سلولها افزایش مییابد و سایر آزمایشات که لزومی برای گفتن همه آنها نیست. تشخیص قطعی با الکتروفورز هموگلوبین انجام میشود که در تالاسمی ماژور هموگلوبین A طبیعی ساخته نمیشود و 98% هموگلوبینها را هموگلوبین F تشکیل میدهد و هموگلوبین A2 نیز تا 5% افزایش پیدا میکند.
عوارض
از عوارض تالاسمی یک سری از عوارض از جمله اختلال رشد و تغییر قیافه بیمار و بزرگی کبد و طحال که به علت خود بیماری است و یکسری عوارض دیگر ناشی از درمان تالاسمی است. اصلیترین این عارضه هموسیدوز یا هموکروماتوز است.
هموسیدروز به رسوب آهن در بافتها گفته میشود که نتیجه غیر قابل اجتناب تزریق طولانی مدت خون است. در هم نیم لیتر خونی که به بیمار تزریق میشود، حدود 200mg آهن به بافتها منتقل میکند که این مقدار آهن نمیتواند از بدن دفع شود و در بافتها رسوب میکند و باعث نارسایی در بافتها میگردد. بخصوص رسوب آهن در قلب و پانکراس و غدد ، مشکل اصلی این بیماران خواهد بود که باعث نارسایی پانکراس و دیابت ، نارسایی قلبی و نارسایی غدد جنسی و تیروئید و ... میشود.
درمان
تالاسمی شدید و درمان نشده همیشه باعث مرگ در دوران کودکی میگردد. در صورت تزریق مکرر خون و حفظ سطح مناسبی از خون میتوان طول عمر ا افزایش داد و تا حد زیادی مانع از تغییرات استخوانی و اختلال رشد گردید. پس درمان تالاسمی عبارتند از:
تزریق دراز مدت خون: هدف از تزریق خون مکرر برای بیمار حفظ هموگلوبین بیمار در سطح بالای 10 است.
دفروکسامین: مشکل اصلی بیماران تالاسمی بعد از سالها ، هموسیدروز و اضافه بار آهن است، که میتوان آن را به کمک تزریق مرتب دفروکسامین به صورت زیر جلدی یا وریدی تخفیف داد. این دارو با آهن ترکیب شده و از ادرار دفع میشود. البته مقدار زیاد این دارو ممکن است باعث واکنش پوستی در محل تزریق و یا عوارض عصبی به ویژه در دستگاه بینایی و شنوایی شود. بنابراین این دارو به تنهایی برای پیشگیری دراز مدت از مسمومیت با آهن کافی نیست.
برداشتن طحال: اگر بزرگی طحال ، نیاز به تزریق خون را بیشتر کند طحال برداشته میشود تا نیاز به خون کاهش یابد.
پیوند مغز استخوان: درمان قطعی بیماری با پیوند مغز استخوان است. البته این عمل با مرگ ومیر بالایی همراه است. و در برخی بیماران نیز سلولهای تالاسمی مجددا رشد میکنند.
روند بیماری
امروزه با توجه به درمانهای موجود بیماران تا 30 سالگی هم زنده میمانند. و اینها بچههایی با رشد ناقص هستند و شایعترین علت مرگ آنها نارسایی قلبی به علت هموسیدروز و همچنین به علت تزریق خون و افزایش بار قلب میباشد.
تالاسمی مینور
تالاسمی مینور معمولا بدون علامت بوده و علایم بالینی واضح ندارند و بطور عمده در تستهای چکاپ به صورت اتفاقی تشخیص داده میشوند. این افراد کم خونی مختصر (هموگلوبین بیش از 10) با سلولهای گلبول قرمز کوچک و کم رنگ (هیپوکروم میکروسیتر) دارند که معمولا مشکلساز نمیباشد.
تالاسمی مینور در نتیجه اختلال یکی از دو ژن سازنده زنجیره گلوبین بتا به وجود میآید که این ژن ناقص یا از پدر و یا از مادر به فرد به ارث رسیده است، در نتیجه کاهش یا فقدان ساخت زنجیره بتا از یک ژن اتفاق میافتد و به دنبال آن هموگلوبین A2 تا حدود %8-4 افزایش مییابد و گاهی افزایش هموگلوبین F در حدود %1-5 دیده میشود.
تنها نکتهای که در تالاسمی خفیف یا مینور جالب توجه است، این است که این افراد موقع ازدواج نباید با یک فرد شبیه خود (تالاسمی مینور) ازدواج کنند.
آلفا تالاسمی
علت آلفا تالاسمی حذف یک یا چند ژن از 4 ژن سازنده زنجیره آلفاست، هر چه تعداد ژنهای حذف شده بیشتر باشد بیماری شدیدتر میشود و براساس تعداد ژنهای حذف شده به 4 گروه تقسیم میشوند.
هیدروپس فتالیس: که حذف هر 4 ژن آلفا را دارند و هموگلوبین ساخته شده فقط از زنجیرههای گاما تشکیل شده است که هموگلوبین بارتز گفته میشود و وخیمترین نوع آلفا تالاسمی است و با حیات خارج رحمی منافات دارد و جنین هنگام تولد مرده است و یا مدت کوتاهی پس از تولد میمیرد. این جنینها دچار ادم شدید هستند.
بیماری هموگلوبین H: که در اثر حذف 3 ژن آلفا گلوبین بوجود میآید. بیماران دچار کم خونی هیپوکروم میکروسیتیک بوده و بزرگی طحال در آنها دیده میشود. در بعضی مواقع ممکن است نیاز به تزریق خون داشته باشند و در صورت کم خونی شدید و نیاز به انتقال خون باید طحال برداشته شود.
صفت آلفا تالاسمی 1: که 2 ژن آلفا حذف شده و از هر لحاظ شبیه بتا تالاسمی مینور است.
صفت آلفا تالاسمی 2: که فقط یک ژن از 4 ژن حذف شده و یک حالت ناقل ژن ، خاموش و بدون علامت است.
 انتخاب جراح بینی - بهترین جراح بینی
انتخاب جراح بینی - بهترین جراح بینی  عکس: استهلال ماه مبارک رمضان
عکس: استهلال ماه مبارک رمضان  عکس: ارزش تیم های حاضر در یورو 2016
عکس: ارزش تیم های حاضر در یورو 2016